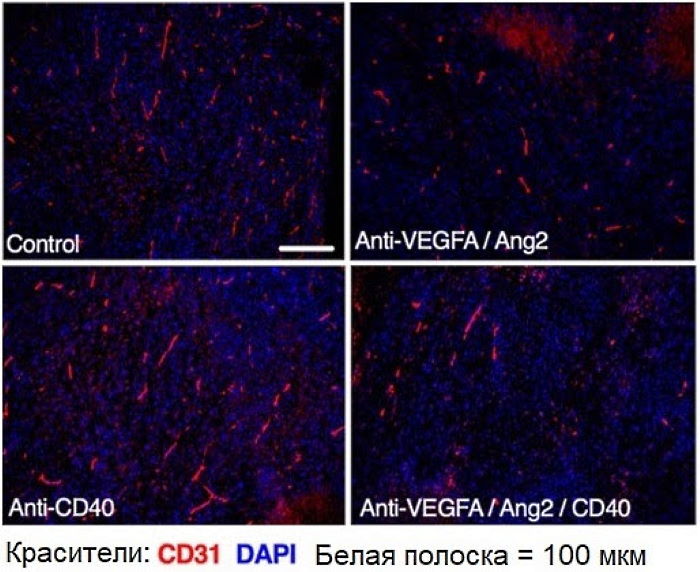
Согласно результатам исследований на животных моделях, проведенных исследователями Университета Базеля, одновременное использование антител, которые проявляют два различных механизма действия, может обеспечить более эффективное разрушение опухолей, чем существующие иммунотерапевтические методы. Новый подход к лечению сочетает в себе антитело CD40 с анти-сосудистым эндотелиальным фактором роста A (анти-VEGFA; бевацизумаб) и антиангиопоэтин 2 (Ang2) антагонистические антитела для стабилизации васкуляризации опухоли. Исследователи предполагают, что эта комбинированная стратегия может принести пользу пациентам, которые не реагируют на существующие методы лечения иммунотерапией рака.
Руководитель исследования Абхишек Кашьяп, доктор медицинских наук, руководитель проекта в отделе биомедицины, считает, что пациенты с “холодными” опухолями — опухолями, которые плохо поддаются иммунотерапии, — могли бы извлечь наибольшую пользу из этого нового комбинированного подхода, который использует дополнительные антиангиогенные агенты. «Наши результаты показывают, насколько важно понимать биологию опухолей», — заявил он. «Антиангиогенные антитела могут сделать «холодные» опухоли «горячими», так что иммунотерапия будет работать лучше.»
Как заключили авторы в своей опубликованной статье в журнале Proceedings of the National Academy of Sciences (PNAS), «анти-CD40 иммунотерапия может представлять собой комплементарный подход к ингибиторам иммунных контрольных точек для комбинации с ингибиторами ангиогенеза … мы считаем наши выводы полезными в свете современных клинических исследований ранней фазы, которые исследуют агонистические анти-CD40 антитела в комбинации с различными антиангиогенными агентами. «Кашьяп и его коллеги сообщили о своих выводах в статье под названием, «Оптимизированное антиангиогенное перепрограммирование микроокружения опухоли потенцирует иммунотерапию CD40.»
В то время как противоопухолевые стратегии, основанные на блокаде иммунных контрольных точек PD-1 и/или CTLA-4, привели к “поразительным” клиническим реакциям у отдельных типов рака, эти иммунотерапии оказались эффективными только у меньшинства онкологических больных, пишут авторы. Таким образом, новые подходы активно исследуются. Антитело, активирующее рецептор CD40 на поверхности иммунных клеток, и, таким образом, стимулирующее выработку естественных киллерных Т-клеток, показало перспективность в доклинических исследованиях. «Агонистическое таргетирование CD40 представляет собой альтернативный подход для укрепления противоопухолевого иммунитета», — отметили исследователи. Однако лечение с использованием антитела CD40 не оправдало ожиданий в клинических испытаниях, и у менее 20% пациентов наблюдался положительный ответ на терапию.
Исследовательская группа по иммунологии рака в Университете Базеля в настоящее время показала на животных моделях, что эффекты антитела против CD40 могут быть значительно усилены путем его объединения с двумя антителами, которые нацелены на опухолевые кровеносные сосуды. Отправной точкой для их исследования было наблюдение, что, хотя введение антител против CD40 действительно приводит к предполагаемому увеличению количества киллерных Т-клеток, эти иммунные клетки могут быть обнаружены только в периферических областях, а не внутри опухоли. Исследователи подозревали, что это связано с природой кровеносных сосудов опухоли. «Обычно кровеносные сосуды опухоли не плотные и протекающие или отстают в своем развитии, — отметил Кашьяп. — Следовательно, нет никакого гарантированного хорошего способа для Т-клеток-киллеров проникнуть внутрь опухоли. Наша гипотеза заключалась в том, что клетки-убийцы способны проникать в опухоль и разрушать ее только при наличии достаточного количества здоровых кровеносных сосудов.»
Исследователи разработали противоопухолевую стратегию, которая сочетала лечение с использованием анти-CD40 антител с антиангиогенными анти-VEGFA и анти-Ang2 антителами, которые могут стабилизировать кровеносные сосуды опухоли. Затем команда испытала эту комбинацию антител на животных моделях для различных типов опухолей, включая колоректальные, грудные и кожные. Как и следовало ожидать, сочетание этих трех антител значительно улучшило разрушение опухолевой ткани при всех видах рака. «Сила нашего исследования заключается в том, что мы получили во многом схожие результаты в различных моделях опухолей и с использованием различных антител, нацеленных на CD40 и VEGFA/Ang2», — пишут исследователи. Более детальный анализ также показал, что улучшенные ответы на лечение являются результатом предсказанного механизма действия, с добавлением двух антиангиогенных антител, гарантирующих, что опухоли сохраняют больше неповрежденных кровеносных сосудов.
Однако, исследование неожиданно также показало, что комбинация антител усиливает иммунную систему несколькими способами, например, поддерживая лучшее проникновение киллерными клетками внутрь опухоли и стимулируя враждебную опухоли воспалительную реакцию в микроокружении опухоли. «Здесь мы показываем, что благодаря синергическим механизмам с антителами, ко-таргетирующими VEGFA и Ang2, терапевтическая эффективность агонистических антител CD40 при различных типах рака у мыши значительно улучшается», — заключили они. «…мы показали, что комбинация агонистических антител CD40 с двойной блокадой VEGFA / Ang2 усиливает противоопухолевый ответ в моделях рака мыши за счет синергической регуляции генов и индукции иммунно-пермиссивного микроокружения опухоли, характеризующегося активацией провоспалительных (M1-подобных) макрофагов, нормализацией сосудов и улучшением инфильтрации и пространственной локализации эффекторных Т-клеток.»
Результаты особенно обнадеживают не только из-за значительных полученных эффектов, но и потому, что несколько других различных лабораторий достигли тех же результатов, предположил Кашьяп. Эксперименты проводились в Университетской больнице Базеля, Политехнической школе Лозанны (EPFL) и Инновационном центре Roche в Цюрихе. «Инновационный и трансляционный потенциал этой работы является результатом тесного и отличного сотрудничества между прикладными и фундаментальными исследованиями, между Базельским университетом и EPFL, а также между академическими кругами и промышленностью, — отметил Альфред Зиппелиус, доктор медицинских наук, профессор трансляционной онкологии Базельского университета и старший автор исследования.
Источник: GEN