Ученые обнаружили небольшую молекулу препарата, который может выключить устойчивость раковых клеток к химиотерапии. Лекарственная устойчивость является основной причиной рецидива рака и ответственна за 90% смертей, связанных с болезнью.
Новое соединение, которое было испытано на животной модели меланомы, смогло значительно поднять эффективность текущих методов химиотерапии. Оно препятствует способности рака выживать, эволюционировать, и приспосабливаться к повреждению ДНК, которые вызывает химиотерапевтические лекарства такие как цисплатин.
«Химиотерапия часто эффективна в первый раз, но затем рак мутирует и становится устойчивым к этому препарату, и в следующий раз терапия не работает», — сказал старший соавтор исследования Пэй Чжоу, к.м.н., профессор биохимии в Медицинской школе Университета Дьюка.
«Это напоминает мне Боггартов, тех оборотней из «Гарри Поттера», которые превращаются из одного страшного существа в другое. Прелесть этого подхода в том, что вы, по сути, замораживаете домового в его нынешнем виде, чтобы убить его навсегда.»
В своей простейшей форме раковые клетки — это нормальные клетки, которые выходят из под контроля. Каждый раз, когда эти клетки делятся, ДНК внутри них должна реплицироваться, чтобы генерировать новые копии, чтобы войти в каждую новую клетку. Первые химиотерапевтические препараты были основаны на том, что быстро растущие раковые клетки будут более чувствительны к повреждению их ДНК. Препараты, подобные цисплатину, предназначены для повреждения ДНК, в результате чего чувствительные механизмы репликации, обычно отвечающие за копирование каждой нити, останавливаются. Если репликация ДНК задерживается слишком долго, клеточное деление останавливается, и клетки умирают.
Стратегия жестока и эффективна, в некоторых случаях даже целебна. Но в долгосрочной перспективе часто терпит неудачу, поскольку раковые клетки находят способ размножаться даже при наличии повреждения ДНК.
«Раковые клетки часто заменяют механизм высокоточного воспроизведения, который обычно отвечает за копирование, небрежной заменой, которая покрывает повреждения и движется дальше», — сказал Чжоу. «В результате клетки выживают, но с мутациями в ДНК.»
Поскольку этот процесс, известный как транслизионный синтез, является основной причиной устойчивости рака к лекарственным средствам, он стал основной областью исследований в области рака. Ученые определили ключевой вовлеченный белок, названный Rev1, и даже разрушили его с помощью генетических средств — работы, выполненные в лабораториях Грэма К. Уолкера и Майкла т. Хеманна в МТИ, обоих старших соавторов этого исследования. Однако попытки сделать то же самое с маленькими молекулами так и не увенчались успехом, вероятно, потому, что белок не имел очевидного связующего кармана, который мог бы использовать потенциальный препарат.
В этом исследовании Чжоу и его коллеги из Дьюка, МТИ и Университета Род-Айленда решили попытать счастья в поиске небольшой молекулы, чтобы блокировать или ингибировать Rev1. Они проверили 10 000 маленьких молекул соединений и были удивлены, обнаружив, что одна молекула под названием JH-RE-06 кажется может сделать трюк.
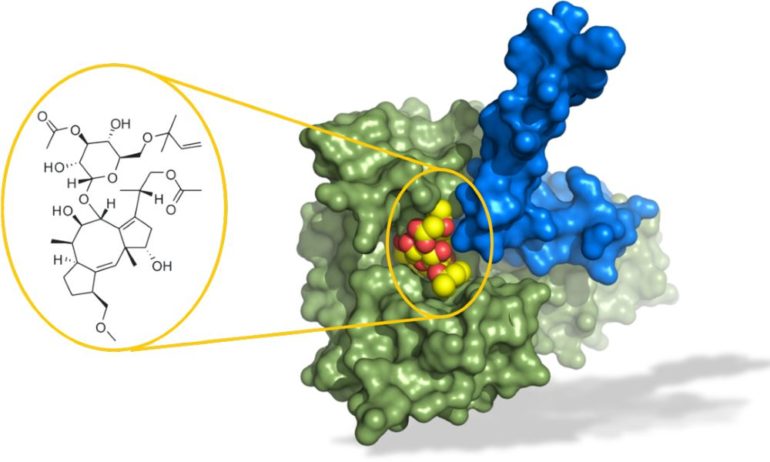
Исследователи использовали метод, называемый рентгеновской кристаллографией, для визуализации неожиданных взаимодействий между Rev1 и JH-RE-06. Они обнаружили, что когда Rev1 взаимодействует с JH-RE-06, он спаривается или димеризуется с другой копией себя, создавая связующий карман, где его раньше не было. Когда Rev1 заперт в этом димере, он больше не может помочь раковым клеткам выжить и достичь их способности к изменению формы.
Затем исследователи протестировали новую молекулу в линиях раковых клеток человека и показали, что она повышает способность нескольких форм химиотерапии убивать клетки, а также подавляет их способность мутировать в присутствии ДНК-повреждающих препаратов. Наконец, они протестировали его на мышиной модели меланомы человека. Они обнаружили, что опухоли не только перестали расти у мышей, получавших комбинацию цисплатина и JH-RE-06, но и что эти мыши выживали дольше.
Старший соавтор исследования Юонг Хонг, к.м.н., профессор химии в Университете Дьюка, сказал, что в настоящее время они создают версии JH-RE-06, которые имеют улучшенные фармакологические свойства, которые могут сделать его еще более привлекательным препаратом. «Это отличное доказательство принципа, что можно нацелиться на этот белок, но у нас есть еще много работы, чтобы превратить это соединение свинца в жизнеспособного кандидата, которого мы можем взять в клинику.»
Источник: Duke University